|
关 键 词:电沉积镍;柠檬酸盐镀液;分散因子;缓冲容量 作 者:李超群,李新海,王志兴,郭华军 内 容: (中南大学冶金科学与工程学院,湖南长沙410083) 摘要:几乎所有的镀镍溶液都用硼酸作缓冲剂,但含硼化合物毒性高。研制了一种适合于电沉积镍的新型电镀溶液,镀液中柠檬酸钠充当缓冲剂和络合剂,这种镀液的缓冲容量比传统Watts大。研究了柠檬酸钠对阴极极化曲线、阴极电流效率、镀液分散因子的影响。用扫描电镜检查:镍沉积层致密、针孔少、结晶细小,X射线分析结果表明,与从Watts镀液中得到的镍沉积层比,从柠檬酸钠镀液中得到的镍沉积层晶粒小,晶面取向随机。因此,在Watts电镀液中,柠檬酸钠是硼酸的有效替代品。 关键词:电沉积镍;柠檬酸盐镀液;分散因子;缓冲容量 中图分类号:TM911.14;TQ153.12文献标识码:A 文章编号:1001-9731(2010)05-0903-04 1引言 镍及镍基合金具有优良的机械加工和防腐性能,因此,常通过电沉积镍及镍基合金的方法制备合适的装饰和功能性金属镀层,用于延长工业、交通和服务设施的寿命,以及用作唱针、电铸印刷板、金属箔、管、薄膜和其它用品。 电镀溶液的选择主要取决于所需镀层的性质和要求。氨基磺酸盐溶液是一种重要的镀镍体系,从该镀液中沉积的镍层具有低内应力和优异的机械性能,但氨基磺酸盐镍价格高,从经济成本角度考虑,所得镀层昂贵。Watts镀液是应用最广的镀镍溶液,它主要包括硫酸镍、氯化镍、硼酸和有机光亮剂等。在氨基磺酸盐和Watts镀液中,硼酸是必不可少的缓冲试剂,但含硼化合物的毒性高。含硼废渣废水排放,使地下水及江河水质受到严重污染,严重影响生态平衡和人类健康。为了减少和消除硼毒的危害,1993年、1998年世界卫生组织先后规定饮用水中的含硼量应低于0.3、0.5mg/L,世界上许多国家也相继制定了饮用水含硼标准,我国也于2002年修订地面水环境质量标准时,首次将硼元素列入“集中式生活饮用水地表水源地特定项目”的80个指标中,规定硼的标准限值为0.5mg/L。 硼常常因岩石风化、海水蒸发、火山运动等自然因素进入环境中,也有许多人为因素引起环境中含硼量增高,镀镍工业废水排放就是加重水资源硼污染的重要因素之一。因此,在镀镍工业上,寻找一种对环境更友好的硼酸替代品是非常必要的,这对降低废水处理成本、保护环境和促进镀镍工业的可持续发展大有裨益。 本文研制了一种新的镀镍溶液:就是用柠檬酸钠取代硼酸作镀液的缓冲剂,柠檬酸钠可用于食品工业,对人体健康、对环境友好,而且价格便宜。比较了柠檬酸钠与硼酸镀液的缓冲容量和分散因子,研究了柠檬酸钠浓度对镀液缓冲容量和分散能力、阴极电流效率、阴极极化曲线的影响。用扫描电镜检查镍沉积层的表面形貌,X射线衍射分析晶体结构。 2实验 2.1电镀溶液 镀镍溶液主要包括硫酸镍、氯化镍、柠檬酸钠、十二烷基硫酸钠,镀液的化学成分见表1,所有镀液都由新制备的去离子水和分析纯化学试剂配制,镀液的pH值用稀硫酸和氢氧化钠调整。
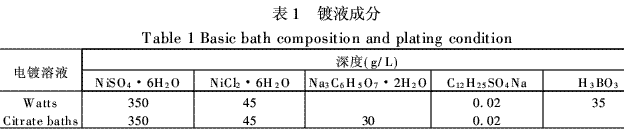
2.2实验过程 阳极用电解镍(60mm×80mm),阴极是低碳钢带,尺寸为40mm×30mm×0.08mm,其成分(%质量分数)是C为0.05~0.11、Si≤0.03、Mn为0.25~0.50、P≤0.035、S≤0.035、Ni≤0.25、Cr≤0.1、C≤0.25,其余是Fe。钢带分别用600、800、1000目砂纸抛光,然后进行化学清洗和电解除油,在7%盐酸溶液中活化处理后就进入镀槽中电镀。电镀完后,冲洗阴极,干燥称重。沉积层的晶体结构由X射线衍射分析确定(D/max2550VB+18kW),表面形貌用扫描电镜观察(JE-OL JSM6380)。 镀液的分散因子用Haring-Blum槽测定。 镀液滴定曲线和缓冲容量的测量:取样100mL用1.0085mol/L标准氢氧化钠溶液滴定,在滴定过程中,不断搅拌溶液,待溶液清亮后再用pHS-25型酸度计测量pH值,以确定滴定曲线,计算出在一定缓冲范围内镀液的缓冲容量。 阴极极化曲线在CHI660A电化学工作站(上海辰华仪器公司生产)上测量,扫描速率0.1mV/s。 3结果和讨论 3.1pH滴定曲线和缓冲容量缓冲容量是衡量缓冲能力大小的尺度,通过滴定分析确定。 图1是pH滴定曲线图,图中曲线1表示不含缓冲剂的镀液滴定曲线,结果表明基本没有缓冲容量。在上述镀液中加入硼酸,镀液的缓冲容量有所增加(曲线2)。另一方面,柠檬酸盐镀液显示了较强的pH缓冲能力(曲线3),特别是在pH值<3时;而在pH值为3~5之间,镀液的缓冲能力显著降低,根据pH滴定曲线和VanSlyke方程,计算出缓冲容量见表2。
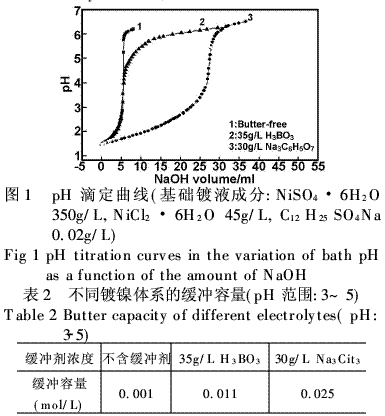
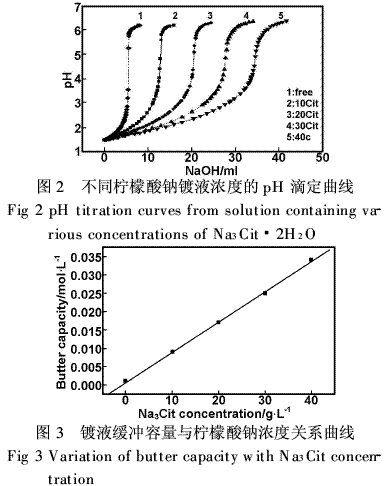
从图1曲线和表2计算结果说明,对于电沉积镍体系,没有缓冲剂的镀液,pH值变化很快,镀液不稳定,容易形成Ni(OH)2沉淀;相比于硼酸作缓冲剂的溶液,柠檬酸钠溶液缓冲容量更大,缓冲能力更强。不同柠檬酸钠含量的镀镍溶液pH滴定曲线和pH在3~5范围内的缓冲容量分别见图2和3。从图3可以看出,随着柠檬酸钠浓度提高,缓冲容量几乎线性增大,溶液的缓冲能力显著提高。
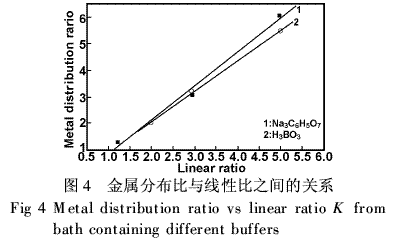
观察pH滴定曲线,在柠檬酸盐镀液中存在有自由的柠檬酸(没有与镍离子形成络合物)和[Ni(HCit)]络合物,它们都能提供H+离子以中和NaOH溶液中的OH-离子,因此,柠檬酸盐镀液的缓冲能力增强。在pH缓冲容量显著减小的溶液pH范围,[Ni(Cit)]-络合物占支配地位,柠檬酸中的所有3个H+离子都发生电离,此时溶液的pH缓冲容量基本丧失。综上所述,柠檬酸钠用作镀镍溶液的缓冲剂,其缓冲容量比硼酸大,镀液不需频繁调整也能得到质量稳定的镀层,并且对环境友好。 3.2分散能力 用分散因子(TI)[9]来表征镀液的分散能力优点是简单、精度高。图4是Watts镀液和柠檬酸钠镀液的金属分布比(M)与线性比(K)之间的关系,从图可以看出M与K之间有很好的线性关系,并且通过M=1、K=1这个代表性的点。
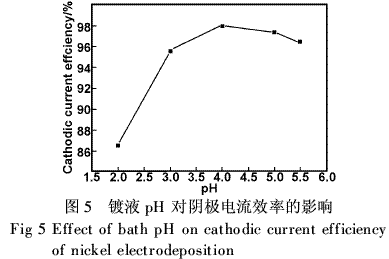
分别求出柠檬酸钠镀液和硼酸镀液的分散因子分别为0.861和0.783,二者相差不大,证明这两种镀液的分散能力相当。 3.3阴极电流效率 测定了在pH为4、温度55℃条件下表1所示化学成分的Watts和柠檬酸钠镀液中沉积镍的阴极电流效率,结果分别为98.26%和97.52%,证明在此条件下,两种镀液的阴极电流效率都高,尽管柠檬酸钠镀液中沉积镍的电流效率略低,但数值相差不大。 在pH值为2.0~5.5范围内,研究了pH值对阴极电流效率的影响,如图5。很清楚,当pH在2~4范围内变化,镍沉积的电流效率随pH值的增加而增加,当pH>4后,电流效率有所下降,在pH=4时,电流效率达到98%。这种变化意味着当镀液的pH值下降,氢气析出反应更容易发生,从而降低了阴极电流效率,这与后面要讨论的pH下降引起阴极极化曲线向负得少的方向变化是一致的,因为pH值减小能降低氢析出反应的过电位。因此溶液的pH值在3~5之间是适宜的。
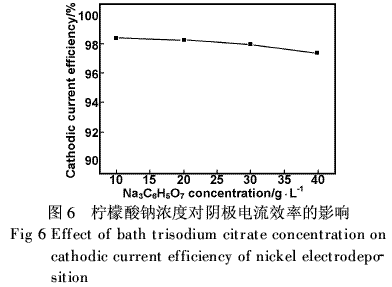
保持镀液中硫酸镍浓度不变,发现阴极电流效率随着柠檬酸根离子的增加而下降(见图6),这个结果证明:柠檬酸根离子浓度增大,镍的络合物增加,自由Ni2+离子浓度降低,析氢副反应加剧。因此,溶液中Ni2+离子浓度与柠檬酸根离子浓度之比(即[Ni2+/[Cit3-])不宜过低。
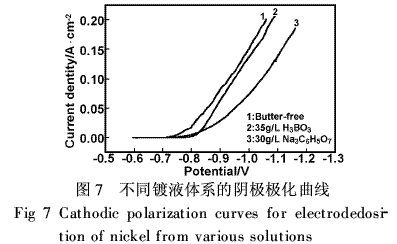
3.4阴极极化曲线 硼酸和柠檬酸钠对在低碳钢带上沉积镍的阴极极化的影响如图7,曲线1表示硫酸镍、氯化镍镀液中的阴极极化,很明显,只有较小的极化电位;加入硼酸到上述镀液中,极化曲线向电位负方向稍有增大(曲线2),硼酸的影响主要是阻挡了镍沉积的活性位置;在上述溶液中加入柠檬酸钠,阴极极化明显加大(曲线3),这种现象是由于柠檬酸根与镍离子形成了可溶性络合物,降低了自由的Ni2+浓度,另外,柠檬酸根离子本身或以金属络合物形式吸附在阴极表面,阻碍Ni2+发生放电的活性点。
从表3镍-柠檬酸盐络合物的稳定常数值可以推出,在溶液中NiCit-是主要的络合物,它的平衡常数值最大,另外,由于柠檬酸钠的浓度低于金属离子浓度,因此在给定的pH条件下,自由的Ni2+浓度也高。
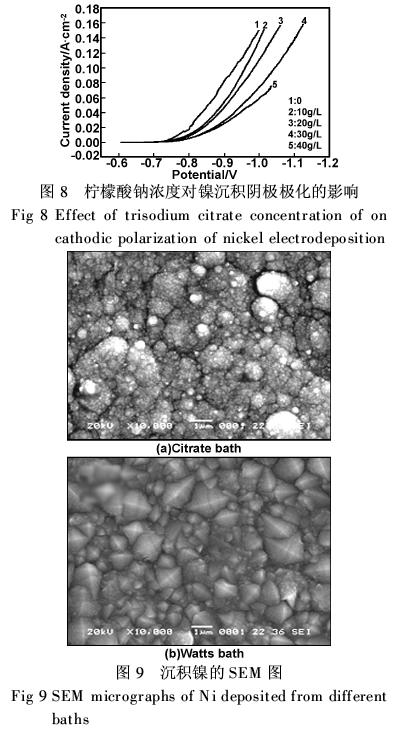
随着柠檬酸根盐浓度加大,更多的Ni2+离子形成络合物,自由Ni2+浓度进一步降低;同时更多的柠檬酸根离子吸附在阴极表面,妨碍Ni2+离子放电,因此,阴极极化会随着柠檬酸盐浓度的加大而增加,在低电流密度区更明显,如图8。 3.5沉积层的表面形貌和结构 通过扫描电镜检查,从柠檬酸盐镀液中沉积的镍均匀分布在阴极钢带上,形状类似“卷心菜”(见图9),结晶颗粒比从Watts镀液中沉积的镍细,因此可推断出:柠檬酸盐镀液中配合物的存在能帮助产生结晶更细小的沉积层。
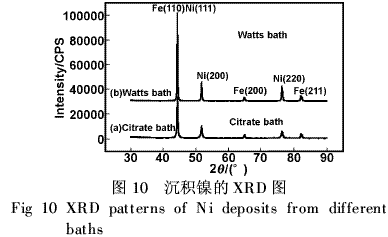
图10是分别从柠檬酸盐和Watts镀液中沉积镍的XRD图,表明从柠檬酸盐镀液中得到的是面心立方结构镍,二者的特征谱线与纯镍一致。但由于镀层只有6μm,不足以阻止X射线通过镍层而显示出基体铁的谱线。
4结论 (1)对于镍沉积,与Watts镀液相比,柠檬酸钠镀液具有更高的缓冲容量、相近的分散因子和阴极电流效率,它是一种实用、有效、对环境更友好的硼酸的替代品。 (2)柠檬酸盐镀液的缓冲容量和阴极电流效率与柠檬酸钠浓度密切相关。柠檬酸钠浓度增大,缓冲容量线性提高,而阴极电流效率降低。 (3)从柠檬酸盐镀液中制备的镍沉积层致密、针孔少,晶粒细,呈“卷心菜”形状和面心立方结构。 参考文献: [1]Supicova M,Roik R,TrnkovaL,et al.[J].J Solid State Electrochem,2006,10:61-68. [2]Supicova M,Rozik R,TrnkovaL,et al.[J].J Solid State Electrochem,2006,10:61-68. [3]Stetten D.[J].Anal Chem,1951,23(8):1177-1179. [4]吴万伟,田宏建.[J].北京师范大学学报(自然科学版),1989,2:50-53. [5]王宏英.[J].表面技术,1994,23(4):176-179. [6]Chadi Y,Wolfram K,Roger C,et al.[J].Environmental Geochemistry and Health,2005,27:419-427. [7]GB3838-2002,地表水环境质量标准. [8]Van Slyke D D.[J].J Bio Chem,1922,52:525-570. [9]Robert V,Jelinek,Hero F.[J].Journal of the Electro-chemical Society,1957,104(5):279-281.[10]Rashwan S M.[J].Metall,1999,53(12):686-691. 注:本站部分资料需要安装PDF阅读器才能查看,如果你不能浏览文章全文,请检查你是否已安装PDF阅读器! |