|
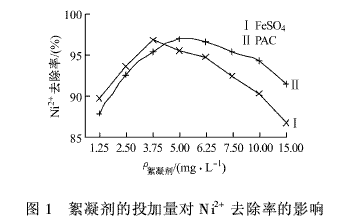
关 键 词:FeSO4,亚铁絮凝,含镍废水 作 者:杨丽芳,张志军,张文波 内 容: (1.苏州市创新净化有限公司,江苏苏州215144; 2.江苏工业学院环境与安全工程学院,江苏常州213164) 摘要:通过正交实验和对比实验考察了两种絮凝剂FeSO4和PAC对废水中低质量浓度的Ni2+的去处效果,主要研究了添加絮凝剂的质量浓度、溶液的pH值、搅拌速率和搅拌时间等因素对去除率的影响,并对絮凝后的污泥性能进行相关实验。结果表明:絮凝处理操作简单,污泥产生量少,工业应用性强,且去除率较高;当溶液的pH值为9.6,FeSO4的质量浓度为3.75mg/L时,Ni2+的去除率平均可达96.8 %以上,而且经FeSO4絮凝后产生的污泥具有一定的絮凝效果,可回流至絮凝工艺段重复使用。 关键词:FeSO4;亚铁絮凝;含镍废水 中图分类号:X 7 文献标识码:A 文章编号:1000-4742(2011)03-0045-03 0 前言 在通常条件下,重金属废水一般采用化学沉淀法去除其中的重金属。但对于微量重金属,因原溶液中离子的质量浓度较低难于生成沉淀,所以采用一般的化学沉淀法效果不佳。但是如果溶液中有一定量的亚铁离子存在时,微量重金属可与其产生共沉淀而被去除。有研究[1]显示,在中性或弱碱性环境中,FeSO4可水解生成Fe(OH)2和Fe(OH)3沉淀。这两种氢氧化物都具有十分庞大的比表面积并带有电荷,可吸附水中各种重金属离子并发生共沉淀;而且对水中的胶体、多相系微粒及各种悬浮物也都有较强的去除能力。当溶液的pH值大于9.5时,亚铁离子可与水中溶解氧迅速发生氧化反应,形成多核羟基配位物铁离子,各种形态的多核羟基铁离子可发挥更好的絮凝、吸附作用,进一步有效去除废水中的微量污染物[2]。 本实验以常州某电镀厂含镍清洗废水为研究对象,以FeSO4和PAC作为絮凝剂,分别考察絮凝剂的投加量、溶液的pH值、搅拌速率和搅拌时间等因素对Ni2+去除率的影响,并对FeSO4,PAC,NaOH等3种药剂进行相关比较和综合效益分析。 1·实验 1.1 实验仪器与药品 MY3000-6型智能混凝实验六联磁力搅拌仪,721型分光光度计,PXS-270型雷磁离子计。NiSO4·6H2O,FeSO4·7H2O,PAC(Al2O3的质量分数≥28 %),NaOH,浓硫酸,以上试剂均为分析纯。 1.2 废水来源及水质 实验所用含镍废水取自常州某电镀厂酸洗后镀铜镀镍的混合清洗废水,其中含有Cu2+,Ni2+,Zn2+,Fe3+,Ca2+等多种重金属离子和SO2-4,NO-3,PO3-3,Cl-等酸根离子,以及少量的Cd2+,Al3+和Mn2+,颜色较深,呈深黄色。具体水质分析结果为:Zn2+49.4 mg/L,Cu2+39.5 mg/L,Ni2+31.7 mg/L,Fe3+775 mg/L,Ca2+113 mg/L,pH值2.03。另外配制Ni2+的质量浓度为50.0 mg/L的模拟废水,质量浓度均为10 g/L的FeSO4和PAC溶液及质量分数为20 %的NaOH溶液。 1.3 实验过程 取800 mL废水,用质量分数为20 %的NaOH调节pH值,开启六联磁力搅拌仪,投加一定量的絮凝剂,搅拌一段时间后,静置30 min,在液面下2 cm处取样测定。 通过3水平4因素的絮凝正交实验,确定了各因素影响FeSO4和PAC絮凝效果的顺序为:溶液的pH值>絮凝剂的投加量>搅拌速率>搅拌时间;并分别考查了絮凝剂的投加量、溶液的pH值、搅拌速率和搅拌时间等因素对实验结果的影响[3]。 2·结果与讨论 2.1 絮凝剂的投加量对Ni2+去除率的影响 取800 mL电镀废水,调节溶液的pH值为9.6,分别投加不同质量浓度的絮凝剂,进行混凝搅拌实验,实验结果,如图1所示。
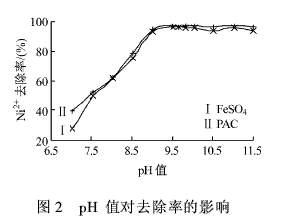
由图1可知:在投加量范围内,Ni2+去除率的曲线均呈先升后降的趋势,FeSO4和PAC的投加量分别在3.75 mg/L和5.00 mg/L时,Ni2+的去除率达到最大值,之后随着絮凝剂的继续加入,去除率均开始下降。对于FeSO4而言,当其投加量过大时,导致溶液的pH值下降,而pH值是FeSO4絮凝的主要影响因素;随着溶液pH值的下降,Ni(OH)2絮体不断减少,同时Fe(OH)2和Fe(OH)3絮体的共存平衡遭到破坏,混凝效果明显下降[4]。而对于PAC而言,过量的PAC会产生过多的矾花絮体微粒,导致沉降速率过慢[5],在静止30 min后溶液中剩余的Ni2+的质量浓度相对较高。本实验中投加过多的絮凝剂不仅造成药剂浪费,而且导致Ni2+去除率下降。所以FeSO4和PAC絮凝Ni2+的最佳投加量分别为3.75 mg/L和5.00 mg/L。 2.2 pH值对Ni2+去除率的影响 在pH值不同的条件下分别加入3.75 mg/L的FeSO4和5.00 mg/L的PAC,在上述搅拌条件下进行混凝实验,实验结果,如图2所示。
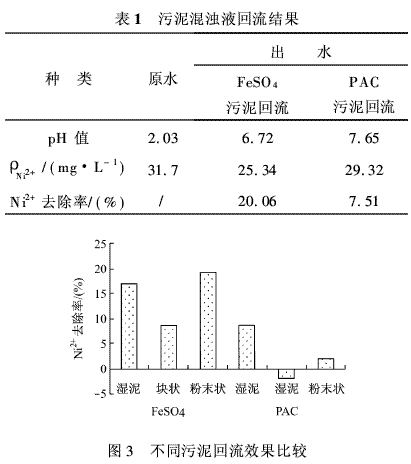
由图2可知:FeSO4和PAC对Ni2+的去除率受pH值的影响均比较大,在pH值为6.5~9.0之间时,Ni2+的去除率增加较快;当pH值分别为9.6和9.5时,Ni2+去除率达到各自的最大值96.87 %和96.97 %,溶液中Ni2+的质量浓度下降到1.0mg/L左右,达到《污水综合排放标准》中的一级排放标准;之后再随着pH值的升高,去除率开始缓慢下降。由此可知:当pH值在9.0~10.5之间时,FeSO4和PAC对Ni2+有较好的絮凝作用。 2.3 搅拌速率和搅拌时间对Ni2+去除率的影响 不同的絮凝剂对搅拌速率和搅拌时间有着不同的要求[6]。分别考查了搅拌速率和搅拌时间对絮凝作用的影响。 根据实验结果综合得出,高速短时较利于PAC对Ni2+的絮凝;低速长时较利于FeSO4对Ni2+的絮凝。FeSO4和PAC絮凝Ni2+的最佳搅拌条件分别为:400 r/min、30 s,100 r/min、10 min,50 r/min、15 min和500 r/min、30 s,150 r/min、5 min,90r/min、10 min。 2.4 污泥对原水中Ni2+的絮凝 因废水中本来就含有大量的铁离子,所以絮凝后污泥中必然也含有大量的铁离子,为了确定经FeSO4絮凝后的污泥是否具有一定的絮凝作用,将其再投加到原水中,对其絮凝性加以考察。另外为了进一步确定污泥中起絮凝作用的是废水中原有的铁离子还是未反应完全的絮凝剂,本实验对FeSO4和PAC絮凝后的污泥混浊液、块状和粉末状的污泥分别进行回流实验,实验结果,如表1和图3所示。
由表1可知:FeSO4絮凝后的污泥具有一定的絮凝能力,但对Ni2+的去除效率较低,仅为20 %左右。由图3可知:粉末状污泥因呈颗粒状而具有较大的比表面积,更能有效发挥残余FeSO4和原废水中铁离子的双重絮凝作用,而湿污泥因絮体颗粒松散导致残余FeSO4和原废水中铁离子的絮凝效果欠佳。由此确定污泥的絮凝作用主要来源于残余的FeSO4和原废水中的铁离子,而原废水中铁离子的絮凝作用是其主要来源。而PAC絮凝后的污泥絮凝作用低,并且絮凝后污泥松散,沉淀速率过慢,溶液浑浊。 2.5 FeSO4,PAC絮凝和NaOH沉淀的比较 2.5.1 最佳pH值范围的比较 分别对FeSO4絮凝、PAC絮凝和NaOH沉淀等3种方法去除Ni2+进行实验研究,并作相关比较。 由实验结果可知:FeSO4和PAC絮凝去除Ni2+的效果均优于NaOH沉淀,去除率平均可提高12 %以上;NaOH沉淀去除Ni2+的最佳pH值区间为9.0~11.0,在pH值为10时,Ni2+去除率达到最大值89.63 %;而FeSO4和PAC在pH值为9.6左右时,Ni2+去除率各自达到最大值,分别为96.87 %和96.97 %。 2.5.2 综合效益分析 由实验数据的相关统计和计算可知:FeSO4价格较便宜,经济适用;结合FeSO4的去除效果、污泥产生量及污泥回流等方面的综合效益[7],其在含镍废水处理方面具有较强的工业实用性。 另外,FeSO4作为絮凝剂在电镀、机械加工、皮革、印染、餐饮等其他工业废水处理中都有较好的效果,它不仅可以去除废水中的重金属离子和胶体微粒,而且对COD,SS,色度,总磷和浊度都有一定的去除效果。 3·结论 (1) FeSO4絮凝处理含镍废水,当pH值为9.6,投加量为3.75 mg/L时,Ni2+去除率平均可达96.8 %以上,出水达到国家排放水质要求。 (2) FeSO4絮凝Ni2+的最佳搅拌条件为400r/min、30 s,100 r/min、10 min,50 r/min、15 min。 (3)经FeSO4絮凝后产生的污泥具有一定的絮凝能力,而且粉末状污泥的絮凝效果高于湿泥和块状污泥的絮凝效果。 (4)相比于PAC,FeSO4价格较便宜,经济适用;结合FeSO4的去除效果、污泥产生量及污泥回流等方面的综合效益,其在含镍废水处理方面具有较强的工业实用性。 参考文献: [1]周继森,易求实.铁盐共沉淀法高效简便去除生活饮用水中的铬[J].湖北教育学院学报,2001,18(2):44-48. [2]邢伟,黄文敏.铁盐除磷技术机理及铁盐混凝剂的研究进展[J].给水排水,2006,32(2):88-91. [3]游晓宏,陈晓琼.混凝技术及其发展[J].工业水处理,2002,22(11):7-9. [4]Li Y, Zeng X, Liu Y,et al. Study on the treatment of copper-electroplating wastewater by chemical trapping andflocculation [J]. Separation and Purification Technology,2003,31(1): 91-95. [5]汤鸿霄.聚合氯化铝与传统混凝剂的凝聚-絮凝行为[J].环境化学,1997,16(6):497-505. [6]李风亭,张善发,赵艳着.混凝剂与絮凝剂[M].北京:化学工业出版社,2005. [7]沈玲.铁盐铝盐絮凝剂的分析比较[J].煤矿环境保护,1993,8(2):46-47. 注:本站部分资料需要安装PDF阅读器才能查看,如果你不能浏览文章全文,请检查你是否已安装PDF阅读器! |