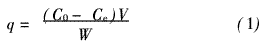关 键 词:微生物吸附材料,Cr(VI),交链包霉, 作 者:黄晓霞,刘茹 摘要:实验采用低质量浓度的Cr(VI)溶液逐级驯化方法,从电镀厂活性污泥中筛选出一株有效吸附Cr(VI)的微生物,经个体、群体形态鉴定,该菌为交链包霉。将该菌扩大培养后采用不同的预处理方法制备成微生物吸附材料,用于处理模拟含铬废水。实验表明:经0.1 mol/L的NaOH处理后的吸附剂对Cr(VI)吸附能力较强,在pH值为2.0,吸附时间为105 min,吸附剂投加量为3.0 g,吸附温度为35℃的条件下,处理含质量浓度为50 mg/L的Cr(VI)废液可达到国家污水综合排放标准。 关键词:微生物吸附材料; Cr(VI);交链包霉 中图分类号:TQ 153 文献标识码:A 文章编号:1000-4742(2011)04-0036-0 0 前言 传统的处理含铬废水的方法主要有化学还原法[1-2]、膜分离法[3]、电解法[4]、吸附法[5]、离子交换法[6-7]等,这些方法不同程度地存在二次污染或成本过高等问题。微生物吸附法具有资金投入少、操作成本低、pH值及温度范围宽、吸附率及选择性高、处理含低质量浓度的金属的废水效果好以及能有效回收一些贵重金属等优点[8]。因此,在处理重金属污染和回收贵重金属方面有广阔的应用前景。 微生物吸附法根据细胞的活性可分为失活微生物法和活体微生物法。活体微生物法受培养条件、菌龄、重金属的质量浓度等诸多因素限制;而失活微生物菌体作为吸附剂与生物的新陈代谢作用无关,具有便于贮藏运输、适应性强、更适合于处理成分复杂、活菌难于适应的工业废水等优点。因此本实验从电镀厂活性污泥中分离出高效吸附铬菌株,制备成失活微生物吸附剂;再根据实际电镀废水中Cr(VI)的质量浓度,研究该生物吸附剂对Cr(VI)的吸附特性,为该菌在实际废水处理中的应用提供理论依据。 1 实验 1.1 实验材料 (1)菌种来源 采自梅州市某电镀厂污水处理活性污泥。 (2)主要仪器 TGL-16型高速离心机,YXQ-LS-50SII型立式压力蒸汽灭菌锅, XSP-4C型生物显微摄影仪,ZD-85型恒温振荡器,722S型可见分光光度计。 (3)主要试剂 牛肉膏,葡萄糖,孟加拉红,蛋白胨,重铬酸钾,二苯碳酰二肼,以上试剂均为分析纯。 (4)培养基 (a)基础培养基 牛肉膏蛋白胨培养基、马丁氏培养基、马铃薯培养基; (b) Cr(VI)筛选培养基 在基础培养基中分别加入含不同质量浓度的Cr(VI)的溶液。 1.2 实验方法 (1)抗性菌株的驯化及筛选 首先,使用Cr(VI)的质量浓度为5 mg/L的初筛基础培养基进行固体驯化培养,采用平板稀释法分离抗性菌株。将初筛得到的纯种菌株分别接种到固体复筛培养基中[Cr(VI)的质量浓度分别为10,20,30,40,50 mg/L],进行逐级驯化,观察生长情况,逐步淘汰抗Cr(VI)能力差的菌株。将筛选得到的高效抗Cr(VI)菌种传代培养,并考察培养后的菌体对水中Cr(VI)的吸附去除性能,以吸附去除性能较好的微生物菌体作为本研究的目标菌种,记录菌种数量和形态特征。本实验微生物的培养条件为28℃,2~5天;吸附实验是在25℃,pH值为2.0的条件下,取20 mL菌液加入到100 mL含50mg/L的Cr(VI)的溶液中,振荡30 min后离心,取上清液测Cr(VI)的质量浓度,测得各菌体对水中Cr(VI)的去除效果。 (2) Cr(VI)的分析方法 实验分析采用二苯基碳酰二肼分光光度法测定Cr(VI)[9]。 (3)生物吸附剂的制备 将筛选得到的优良菌株分别采用不同的预处理方法制备成生物吸附剂。表1是各种处理方法的实验条件。 (4)吸附实验 考察了在100 mL含Cr(VI)的质量浓度为50mg/L的溶液中,吸附剂的用量、pH值、接触时间、温度以及处理方法对吸附量的影响,并用下式计算生物吸附剂的吸附量:
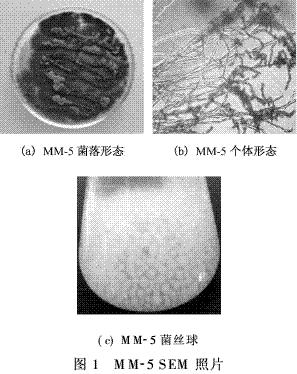
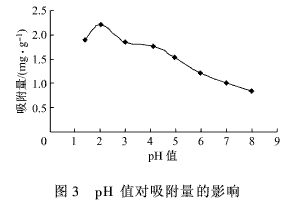
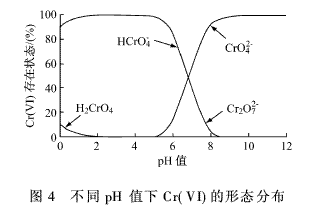
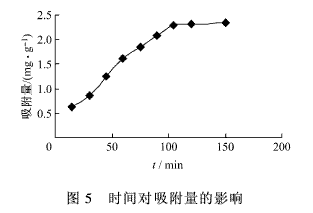
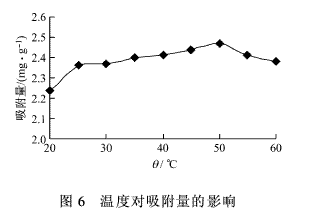
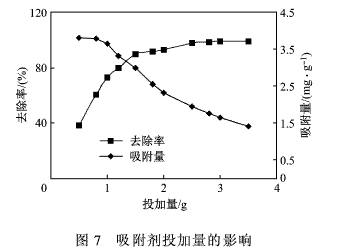
式中:q为吸附量,mg/g;C0为吸附前溶液中的Cr(VI)的质量浓度,mg/L;Ce为吸附平衡后溶液中的Cr(VI)的质量浓度,mg/L;V为溶液的体积,L;W为生物吸附剂的质量,g。 2 结果与讨论 2.1 菌种的筛选与鉴定 经过逐级提高Cr(VI)的质量浓度筛选得到的菌种对水中的Cr(VI)均有一定的去除效果,其中以马丁氏培养基培养出的一株菌种对Cr(VI)的去除率最高,将其命名为MM-5。将分离纯化后的MM-5菌株根据个体、群体特点按文献[10]进行鉴定。该菌落在马丁氏培养基平板上生长24 h后,在平板表面先是长出白色的菌丝,然后随着时间的延长,菌丝的上面长出绿色的孢子,孢子的颜色也渐渐的加深;72 h后菌落蔓延了整个平板,呈致密绒状,中央稍隆起,表面呈近墨绿色,如图1(a)所示。取菌丝于显微镜下观察,营养菌丝无色,没有横隔,其顶端形成分生孢子链,孢子的形状有圆形,有椭圆形,如图1(b)所示。该菌在液体培养基中培养12 h后开始形成菌丝球,其过程是:孢子互相凝聚形成晶核,由孢子生成的菌丝不断地缠绕在晶核上,进而形成较大的菌丝球[11],如图1(c)所示。根据以上特征,经查阅有关文献,将该菌株鉴定为交链包霉。 2.2 制备方法对Cr(VI)吸附的影响 采用5种不同的方法处理经马丁氏培养液在28℃的条件下培养72 h后所得的MM-5菌丝球。取2.0 g经不同方法处理后所得的MM-5微生物吸附剂加入到100 mL含Cr(VI) 50 mg/L的锥形瓶中,在35℃条件下振荡150 min,离心取上清液,测Cr(VI)的质量浓度,并计算吸附量,实验结果,如图2所示。 由图2可知:经0.1 mol/L的NaOH处理后的MM-5微生物吸附剂对Cr(VI)的吸附效果最好。其原因可能是碱处理可以去除细胞壁上的无定形多糖,同时可以溶解细胞上一些不利于吸附的杂质,暴露出细胞上更多的活性结合点,使吸附量增大[12]。 2.3 吸附条件对Cr(VI)吸附的影响 2.3.1 pH值的影响 在不同pH值条件下做吸附实验,称取2.0 gMM-5微生物吸附剂,加入到100 mL含Cr(VI)50 mg/L的溶液中,在35℃下振荡150 min后,离心取上清液,测Cr(VI)的质量浓度,计算吸附量,实验结果,如图3所示。 由图3可知:随着pH值的变化,吸附剂对Cr(VI)的吸附量先上升后下降,存在最大值。这是因为溶液的pH值影响微生物吸附剂的重金属吸附位点和Cr(VI)的化学状态。pH值较低时,细胞壁的功能基团被质子化,由于静电吸引力的作用使Cr(VI)靠近微生物细胞,吸附量较大。在不同pH值条件下,Cr(VI)在溶液中的存在形态,如图4所示[13]。由图4可知:吸附过程中Cr(VI)主要是以HCrO-4的形态与MM-5微生物吸附剂作用,所以当pH值为2时吸附存在最大值。 2.3.2 吸附时间的影响 称取2.0 g MM-5微生物吸附剂,加入到pH值为2.0,100 mL含Cr(VI) 50 mg/L的溶液中,在35℃下振荡一定时间后,离心取上清液,测Cr(VI)的质量浓度,计算不同时间下Cr(VI)的吸附量,实验结果,如图5所示。 由图5可知:随着振荡时间的延长,Cr(VI)的吸附量逐步提高,当吸附时间达到120 min时,MM-5微生物吸附剂对Cr(VI)的吸附量为2.310mg/g,此后再延长吸附时间,吸附量增加不大。综合考虑,吸附时间定为105 min。 2.3.3 温度的影响 称取2.0 g的MM-5微生物吸附剂,加入到pH值为2.0,100 mL含Cr(VI) 50 mg/L的溶液中,在不同的温度下振荡105 min后,离心取上清液,测Cr(VI)的质量浓度,计算Cr(VI)的吸附量,实验结果,如图6所示。 由图6可知:在20~50℃范围内,升高温度对吸附有利,MM-5微生物吸附剂对Cr(VI)的吸附量从2.240 mg/g增加到2.470 mg/g,但增加趋势较为缓慢;继续升高温度,吸附量稍有下降。考虑到能耗,实验温度采用35℃。 2.3.4 吸附剂投加量的影响 准确称取一定量的MM-5微生物吸附剂,加入到pH值为2.0,100 mL含Cr(VI) 50 mg/L的溶液中,在35℃下振荡105 min后,离心取上清液,测Cr(VI)的质量浓度,计算Cr(VI)的吸附量和去除率,实验结果,如图7所示。 由图7可知:MM-5微生物吸附剂投加量越大,去除率越高,但吸附剂的吸附量降低,这说明去除率的增加主要是因为吸附剂用量的增加。经综合考虑,本实验选择3.0 g作为吸附剂投加量。 3 结论 (1)本实验采用含低质量浓度的Cr(VI)的溶液逐级驯化法,从电镀污泥中分离得到对Cr(VI)有较强吸附能力的菌株,经鉴定为交链包霉,将其命名为MM-5。 (2)预处理对吸附效果有不同的影响,经0.1mol/L的NaOH处理后的MM-5微生物吸附剂对Cr(VI)的吸附量较其它处理方法的吸附量大,达到2.350 mg/g。 (3)通过吸附实验确定该微生物吸附剂的最佳吸附条件为:pH值2.0,吸附时间105 min,吸附剂投加量3.0 g,温度对吸附影响不大,从实际出发选择吸附温度为35℃。 参考文献: [ 1 ]张志军,李玲,朱宏,等.化学沉淀法去除电镀废水中铬的实验研究[J].环境科学与技术,2008,31(7):96-97. [ 2 ]刘存海,王廷平,廖全义.镀铬废水中铬的回收及在铬鞣中的应用[J].电镀与涂饰,2007,26(4):52-54. [ 3 ]Yang X J,Fane A G,Macnaughton S. Removal and recoveryof heavy metal from wastewaters by supported liquidmembranes[J].Water Science and Technology,2001,43(2):341-348. [ 4 ]刘铮,韩国成,王永燎.钛-铁双阳极电絮凝法去除电镀废水中的Cr(VI)[J].工业水处理,2007,27(10): 51-54. [ 5 ]刘守新,陈孝云,陈曦.表面酸碱2步改性对活性炭吸附Cr(Ⅵ)的影响[J].环境化学,2005,26(6):91-93. [ 6 ]范力,张建强,程新,等.离子交换法及吸附法处理含铬废水的研究进展[J].水处理技术,2009, 35(1): 30-33. [ 7 ]吴克明,石瑛,王俊,等.离子交换树脂处理钢铁钝化含铬废水的研究[J].工业安全与环保,2005,31(4):22-23. [ 8 ]王建龙,韩英健,钱易.微生物吸附金属离子的研究进展[J].微生物学通报,2000,27(6):449-452. [ 9 ]奚旦立,孙裕生,刘秀英.环境监测[M].北京:高等教育出版社,2004:559-562. [10]魏景超.真菌鉴定手册[M].上海:上海科学技术出版社,1979:563-566. [11]董新姣.一株高耐铜菌株的分离及特性的研究[J].环境保护科学,2003,29(1):16-19. [12]吴涓,李清彪,邓旭,等.白腐真菌吸附铅的研究[J].微生物学报, 1999,39(1):87-90. [13]杨峰.含铬废水生物处理的基因工程菌的构建、性能及机理研究[D].广州:暨南大学,2006:5.
|